La
bronchiolite
(Parte
seconda)
Clinica
Pediatrica, IRCCS Burlo Garofolo, Trieste
E mail:marzia_lazzerini@libero.it.
TUTTE
LE EVIDENZE ED I COMMENTI SULL'USO DI:
- ADRENALINA - nella prima parte - Medico e Bambino, pagine elettroniche; Apr. 2004, 8(4)
Nella
seconda parte
Nella
terza parte -disponibile prossimamente
- BETA -2 STIMOLANTI
- SOLUZIONE IPERTONICA
- FISIOTERAPIA TORACICA
Nella
quarta parte-disponibile prossimamente
- RIBAVIRINA
- IMMUNOGLOBULINE
Le
metanalisi negano un'efficacia clinicamente rilevante
Abbiamo
rilevato in letteratura 4 metanalisi, non altri RCT recenti. Le
metanalisi si riferiscono per la maggior parte all'uso degli
steroidi sistemici.
Metanalisi
1
Garrison
MM, Christakis DA, Harvey E, Cummings P, Davis RL. Systemic
corticosteroids in infant bronchiolitis: A meta-analysis. Pediatrics.
2000;105(4):E44
include 6
studi, relativi solo all'uso di steroidi SISTEMICI.
Risultati:
Durata dell'ospedalizzazione e durata dei sintomi
Nel
complesso i bambini che hanno ricevuto gli steroidi hanno una durata
dell'ospedalizzazione e dei sintomi più breve (risparmio
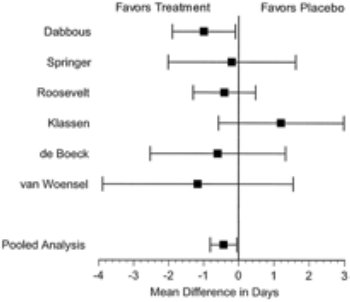
0.43 giorni, IC 95% -0.81 a -0.05 giorni) (Figura
1). Tuttavia l'analisi secondaria che valuta i 5 studi in cui
vengono descritti chiaramente i metodi di randomizzazione, i 5 trial
che misurano la durata dell'ospedalizzazione, e i 4 trial che
escludono i bambini con precedente wheezing, conclude per una
differenza non significativa (rispettivamente -0.43 giorni, IC 95%
-1.05 a +0.18; -0-35 giorni, IC 95%-0.84 a +0.14; -0.29 IC 95% -0.71
a +0.13) (Tabella
1)
Analysis
Performed | Mean*- | Power
CI | Upper
CI | P
Value | Number
of Studies | Included |
All
studies, pooling LOS and DOS | - .43
d | -.81 | -.05 | .03 | 6 | Dabbous,
de Boeck, Klassen, Roosevelt, Springer, van Woensel |
Only
studies for which randomization methods were clearly identified | - .35
d | -.84 | .14 | .17 | 4 | de
Boeck, Klassen, Roosevelt, van Woensel |
Studies
which measure LOS only | - .43
d | -1.05 | .18 | .17 | 5 | Dabbous,
de Boeck, Klassen, Springer, van Woensel |
Only
studies which clearly exclude patients with previous wheezing | - .29
d | -.71 | .13 | .18 | 4 | de
Boeck, Klassen, Roosevelt, Springer |
* A
negative mean favors treatment; a positive mean favors the
placebo. | ||||||
Risultati:
Score clinico: Valutato in 3 trial, i risultati a 24 ore
favoriscono lo steroide (differenza media standardizzata con
diminuzione dello Score -1.6 punti, Ic 95% -1.9 a -1.2)
(Nda: per
confrontare Score Clinici è stata fatta una media
standardizzata, che tuttavia è difficile da interpretare come
rilevanza clinica, poiché non sono espressi gli intervalli di
riferimento)
Metanalisi
2
Lozano
JM Bronchiolitis. Clin Evid. 2004;(12):370-84
include
la precedente review, 6 RCT addizionali e 5 RCT successivi, relativi
a steroidi SITEMICI ed INALATORI.
Risultati:
Benefici
Viene
riportata la precedente metanalisi (Garrison 2000), ma solo in
relazione all'analisi secondaria, statisticamente non significativa
per efficacia dello steroide (vedi sopra). Non è ben chiara la
rilevanza del beneficio sullo score clinico in relazione al fatto che
diverse scale vengono comparate tra loro (NdA: e non viene citata
l'ampiezza della scala standardizzata). Tutti i 6 RCT addizionali e
3 su 5 RCT successivi non riscontrano un vantaggio dello steroide
sugli score clinici e, nelll'unico studio in cui si osserva un
miglioramento dello score, questo è osservabile ad un unica
rilevazione. (Tabella 2)
Ref. | Allocation
/ Blinding | Intervention | Number
of Children | Outcome | Results |
30 | Random
/ blinded | Nebulized
budesonide | 40 | Clinical
score and condition at 6 months | No
benefit |
31 | Random
/ blinded | Prednisolone
/ methylprednisolone | 147 | Hospital
stay; supportive measures in hospital; condition ad 1 month and 1
year after discharge | No
benefit |
32 | Random
/ blinded, factorial design | Desamethasone
/ placebo
Salbutamol/placebo | 32 | Clinical
score and hospital stay | No
benefit |
34 | Random
/ blinded | Prednisolone | 95 | Duration
of ilness after hospitalization | No
benefit |
35 | Random
/ blinded | All
had salbutamol; prednisone | 38 | Clinical
score; oxygen saturation; condition at 7 days and 2 years later | No
benefit |
37 | Random
/ blinded | Betamethasone | 297 | Nine
respiratory tract signs; fever and complications after admission | No
benefit |
37 | Random
/ blinded | All
children received salbutamol (oral or inhaled) prednisolone | 48 | Bronchiolitis
score at day 2 | Transient
effect only on day 2 |
33 | Random
/ blinded | Budesonide | 161 | Hospital
stay; time taken to be symptom free; readmission rates; GP
consultation | No
benefit |
38 | Random
/ blinded | Oral
dexemethasonne | 70 | Clinical
score and admission rate | Improvement
iin clinical score and admission rate |
39 | Random
/ blinded | iv
dexamethasone / placebo | 41 | Number
ventilator, ICU, or hospital days | No
benefit |
40 | Random
/ blinded | iv
dexamethason | B2 | Duration
of mechanical ventilation | No
benefit |
GP,
general pratictioner;ICU,intensive care unit; Ref, reference | |||||
Risultati: Effetti a lungo termine dello steroide
Vengono
inclusi 3 piccoli trial con lungo follow- up (3 anni), che hanno
valutato, con intervista telefonica, gli effetti dello steroide nella
prevenzione degli episodi di wheezing successivi alla bronchiolite.
Due di questi trial non riportano alcuna efficacia dello steroide, il
terzo trial è uno studio in aperto con vari problemi
metodologici
Risultati:
effetti collaterali
Non
vengono descritti negli studi inclusi.
Metanalisi
3
King
VJ, Viswanathan M, Bordley WC, et al. Pharmacologic treatment of
bronchiolitis in infants and children: a systematic review. Arch
Pediatr Adolesc Med 2004;158:127–37.
include 5
RCT su steroidi ORALI (1 RCT addizionale con follow-up a 5 anni), 2
RCT su steroidi PARENTERALI, 6 RCT su steroidi INALATORI. I risultati
sono riportati come descrizione dei singoli studi.
Risultati:
steroidi orali (Tabella
3)
- Tasso di ospedalizzazione: valutato in 2 studi su 6, con beneficio dello steroide in uno studio (nel secondo RCT non è specificato se i risultati sono statisticamente significativi).
- Durata dell'ospedalizzazione: valutata in 2 studi su 6: in uno studio non efficacia dello steroide, nel secondo efficacia solo nel gruppo di pazienti ventilati (senza efficacia sullo score clinico).
- Score Clinico: valutato in 5 studi su 6: non efficacia in 4 studi, nel quinto efficacia solo a 2° giorno, ma non al 3° e 6°, nel sesto efficacia solo per i pazienti non ventilati.
Risultati:
steroidi parenterali (Tabella
3)
Nei 2
studi sul desametasone EV e IM non si osserva un beneficio dello
steroide né sulla durata dell'ospedalizzazione né
sulla durata dei sintomi.
Risultati:
steroidi inalatori (Tabella
3)
Questi
studi sono in media di qualità inferiore a quelli sugli
steroidi orali e parenterali. Lo steroide inalatorio è stato
somministrato per un intervallo variabile tra 2 settimane e 3 mesi, e
gli outcome sono stati valutati ad intervalli più lunghi
rispetto agli studi sugli steroidi sistemici. In pratica si và
a valutare se l'uso degli steroidi inalatori è in grado di
prevenire il broncospasmo e/o la tosse che possono seguire ad un
episodio di bronchiolite.
Dei 6
studi 5 valutano come steroide la budesonide, uno il fluticasone. Uno
degli studi sulla budesonide (Kajosaari 2000) ha osservato una minore
necessità di terapia sintomatica a 2 anni dall'entrata nello
studio per il gruppo che ha usato la budesonide per 2 mesi vs il
gruppo che ha usato la budesonide per 7 gg. Nessun altro degli studi
sulla budesonide ha dimostrato l'efficacia del trattamento. Inoltre
in due studi viene osservato un peggioramento nel gruppo trattati,
misurato come “ wheeze” o tosse ad 1 anno o tasso di riammissione
a 6 mesi.
Un
piccolo studio sul fluticasone somministraro per 3 mesi ha dimostrato
una diminuzione nella tosse notturna a 3 settimane rispetto ai non
trattati, ma non vi è differenza sulla tosse complessiva ed il
wheezing a 3, 6, 12 o 24 settimane.
Risultati:
effetti collaterali (Tabella
3)
Non
descritti nella maggior parte degli studi. In uno dei 2 studi sugli
steroidi parenterali (desametasone) la valutazione del sangue nelle
feci rileva 2/65 episodi nei trattati vs 1/53 nei non trattati. Uno
degli studi sugli steroidi inalatori (fluticasone) rileva 2 casi di
candidasi orale nei 20 trattati vs 0/21 non trattati. Uni studio
sulla budesonide inalatoria a lungo termine non rileva differenza
sulla velocità di crescita a 6 mesi.
Source | Quality
Category | Intervention
and comparison | Patients,
No.* | Primary
Outcames | Significant
Outcomes Differences | Adverse
Effects Reported |
Oral
Corticosteroids | ||||||
Berger
et al. 1998 | Good | Prednisone
vs. Placebo | 38 | Hospitalization | 25%
in prednisone group vs 11% in placebo group; no P value given | Not
reported |
Goebel
et al. 2000 | Good | Prednisolone
+ albuterol vs. placebo + albuterol | 48
(32 with complete data) | Clinical
score
Clinical
score on days 0,2,3 and 6 | None
Both
gorups improved on day 2 compared with day 0 only | 1
Child jittery in prednisolone + albuterol group; resolved after
reduction in albuteral dose |
Klassen
at al. 1997 | Excellent | Dexamethasone
vs placebo | 67 | Duration
of hospitalization, readmission ans need for outpatient
treatment.
Clinical
score change from baseline at 12, 24,36, 48 and 60 h | None
None | Not
reported |
Schuh
et al. 2002 | Excellent | Dexamethasone
vs placebo | 67 | Rate
of hospitalization
Clinical
score form baseline to day 7 | Lower
in dexamenthasone group (19% vs 44%)
None | Not
reported |
van
Woensel et al. 1997 | Fair | Prednisolone
vs placebo | 27
Completed 5-y study | Transient,
persistent, or late-onset wheezing at age 5 y | None | None
observed |
van
Woensel et al. 2000 | Good | Prednisolone
vs placebo | 53 | Duration
of hospitalization in: -Ventilated patients
-Non
ventilated patients
Clinical
score in nonventilated patients | Fewer
days in prednisolone group
None
Improved
in prednisolone group | 1
deadth unrelated to intervention
|
Parental
corticosteroids | ||||||
de
Boeck et al. 1997 | Fair | Dexamethasone
vs placebo | 29 | Duration
of hospitalization
Clinical
score | None
None | Not
reported |
Roosvelt
et al. 1996 | 118 | Dexamethasone
vs placebo | 118 | Time
to resolution
Duration
os oxygen therapy | None
None | Occult
blood in stool seen in both groups, 2/65(treatment) vs 1/53
(placebo) |
Inhaled
Corticosteroids | ||||||
Cade
et al. 2000 | Good | Nebulized
budesonide vs veihicle placebo | 161 | Duration
of hospitalization
Readmission
for respiratory illness within 12 mo
Coughing/weezing
episodes at 12-mo follow-up | None
None
None | Not
Reported |
Fox
et al. 1999 | Fair | MDI
budesonide vs placebo | 49 | Wheezing/coughing
symptoms at 1,2,6 and 12 mo
Hospitalization
in 12 mo | Worsened
for budesonide group at 12 mo
None | mild
cough and wheeze in 1 child in budesonide group; 1 admission for
viral gastroenteritis in placebo group |
Kajossari
et al. 2000 | Poor | Inhaled
buesonide x 7 d vs inhaled budesonide x 2 mo vs symtomatic usual
treatment | 109 | Need
for asthma inalation therapy at 2 y | Budesonide
groups had less need (37% in symptomatic treatment vs 18% in
budesonide for 7 days vs 12% in budesonide for 2 mo groups) | Not
reported |
Reijonen
et al. 1996 | Fair | Inhaled
budesonide vs inhaled cromolyn sodium vs no treatment control | 92 | Days
of symptomatic wheezing at 1 vs 4, 5 vs 8, 9 vs 16 and 13 vs 16
wk | None | Not
reported |
Richter
ans Seddon 1998 | Good | Nebulized
budesonide vs placebo | 40 | Days
and oxygen
Prevalence
of wheezing and use of bronchodilatators during 6-mo follow up
Duration
of hospitalization
Hospital
readmission for respiratory problems | None
None
None
More
readmissions in budesonide group | Median
growth 0.43 cm/mk (budesonide) vs 0.47 cm/wk (placebo); P = .16 |
wong
et al. 2000 | Good | MDI
fluticasone propionate vs placebo | 41 | Overnight
oxygen saturation
Night
cough episodes at 3,6,12,24 and 36 wk
Parent-reported
symptom frequency | None
Better
for fluticasone group at 36 wk only
None | Oral
candidiasis in 2 fluticasone grooup patients |
Abbreviations:
-
MDI, metered dose inhaler
-
*number of patients completing the study | ||||||
Metanalisi
4
Patel
H, Platt R, Lozano JM, Wang EEL. Glucocorticoids for acute viral
bronchiolitis in infants and young children. The Cochrane Database of
Systematic Reviews 2004, Issue 3. Art. No.: CD004878. DOI:
10.1002/14651858.CD004878.
13 RCT
sugli steroidi SISTEMICI, di cui tutti gli studi inclusi in Garrison
2000, per 1198 bambini totali.
Caratteristiche
degli studi e dei pazienti inclusi
- Età bambini: da 0-30 mesi
- Test per VRS : in 10 studi (incidenza di VRS positivi tra 6-100%)
- Bambini con precedenti episodi di wheezing: questa informazione è riferita in 10 studi, solo 7 studi fanno riferimento a popolazione di “first time wheezers”;
- Setting: unità di ricovero pediatriche (10 studi) e pronto soccorso (3 studi)
- Tipi, dosi, durata steroidi:
- in 5 studi desametasone (OS, EM, EV), dosi 0.1-1mg/kg/die, per 3-4 gg;
- in 5 studi metilprednisone, prednisolone o prednisone, dosi tra 0-5-1.5 mg/kg/die, durata tra 2 e 7 giorni;
- in uno studio idrocortisone in infusione continua a 1 mg/kg/ora;
- in uno studio il betametasone IM tra 0.5 a 1mh/5 lbs per 3 gg.
- Dimensione del campione: molto variabile (da 29 a 297 bambini)
- In uno studio sono inclusi anche pazienti in ventilazione meccanica, che sono stati esclusi dalla metanalisi.
- Intervento di controllo: placebo o soluzione fisiologica, in uno studio è stato usato il chinino.
- Co-interventi: terapia di supporto (ossigeno, fluidi) in tutti gli studi. In 8 studi broncodilatatori (salbutamolo eccetto in uno studio adrenalina). In 2 studi non vengono riportati i cointerventi
- Outcomes riportati: durata dell'ospedalizzazione, durata dell'episodio, score clinico. In alcuni studi altri outcome minori come la frequenza respiratoria, la saturazione dell'emoglobina, l'impressione generale del medico sul bambino, il numero di ritorni e di seconde ospedalizzazioni
- Qualità degli studi: 8 studi con punteggio tra 4-5 alla scala Jadad, 2 studi con punteggio 3-5, uno studio 3-4, uno studio 2-3.
Sponsorizzazioni:
non menzionato nella metanalisi
Risultati
Durata
dell'ospedalizzazione (7 studi): non differenza significativa tra
steroide e placebo (differenza media -0.38 giorni, IC 95% -0.81 a +
0.05)
ANALISI
PER SOTTOGRUPPI
- Bambini RSV positivi vs RSV negativi
- Bambini < 12 mesi vs > 12 mesi
- Firt time wheezers vs recurrent wheezers
- dosi prednisone od equivalenti tra 0.1-2 mg/kg/gg vs > 2mg /kg/gg
- dosi totali di prednisone od equivalenti durante il trattamento < 6mg /kg vs 6-30 mg/kg
- Effetto statisticamente non significativo in tutti i sottogruppi, eccetto che:
- nei RSV positivi (differenza media pesata -0.76; IC 95% -1.11 a -0.24) (Tabella 4)
- per dosi totali di prednisone equivalente > 6 mg/kg (differenza media pesata -0.46, IC: 95% -0.9 a -0.03). (Tabella 5)
- Clinical Score al terzo giorno (8 studi): non differenza significativa tra steroide e placebo(differenza media standardizzata -0.20 giorni, IC 95% -0.73 a 0.32).
ANALISI
PER SOTTOGRUPPI (come sopra + sottogruppo aggiuntivo, ovvero pz
ospedalizzati vs gruppo misto ospedalizzati e non ospedalizzati)
- Effetto statisticamente non significativo in tutti i sottogruppi.
- Frequenza respiratoria (6 studi) e saturazione emoglobina (3 studi): non differenza significativa tra steroide e placebo
- Co-interventi (ossigeno, fluidi, broncodilatatori) usati similmente tra gruppi trattamento e placebo (11 studi).
- Tasso di ospedalizzazione (3 studi): non differenza significativa tra steroide e placebo (OR 1.05 , IC95% 0.23 a 4.87).
- Tasso di ritorni per seconda visita in ospedale (3 studi): differenza significativa tra steroide e placebo solo in 1 studio.
- Tasso di riammissione in ospedale (6 studi): non differenza significativa tra steroide e placebo.
- Effetti collaterali (1 solo studio):
- tremori in 2 pz trattati in concomitanza con salbutamolo inalatorio
- sangue occulto nelle feci 2/65 trattai con desametasone EV vs 1/53 in placebo.
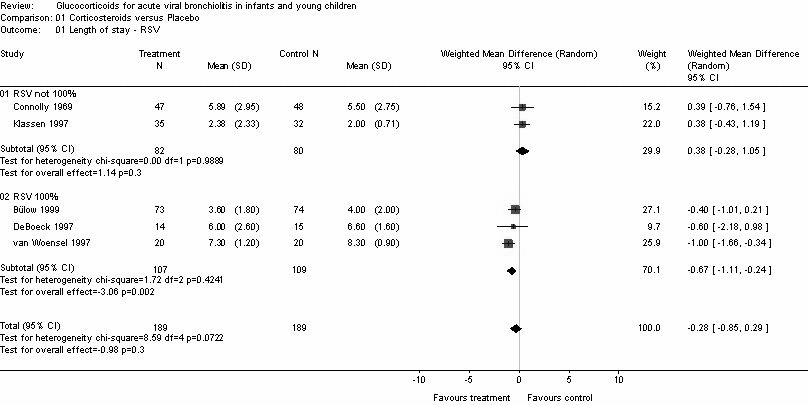
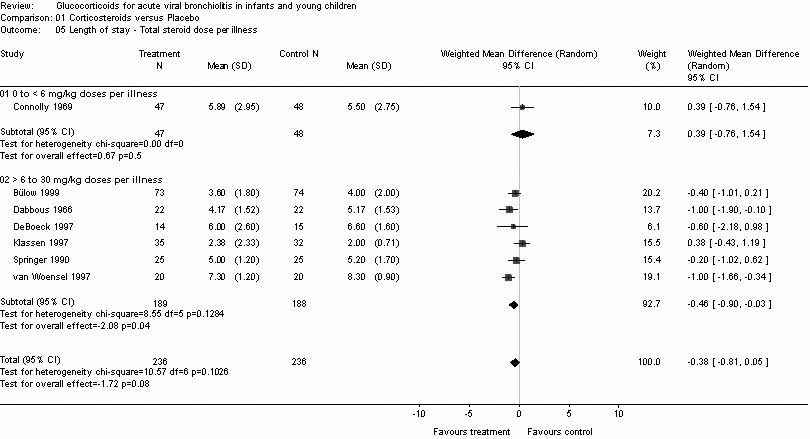
LE
CONCLUSIONI DEGLI AUTORI
Il
trattamento dei bambini con bronchiolite rimane problematico.
Teoricamente gli steroidi potrebbero essere di beneficio riducendo la
componente infiammatoria dell'infezione virale nelle basse vie
aeree, in particolare se utilizzati in fase precoce, prima
dell'avvenuta necrosi cellulare.
Tuttavia
i risultati di questa revisione non mostrano la chiara efficacia
dello steroide sistemico rispetto al placebo. L'efficacia degli
steroidi sembra essere molto limitata, ovvero nei termini di
risparmio medio possibile di 0.38 giorni (9 ore) di ospedalizzazione
per ogni episodio. E' discutibile che questa efficacia sia
clinicamente rilevante. Non sembra inoltre esserci nessun vantaggio
sugli altri parametri, ovvero lo score clinico, la saturazione di
ossigeno, etc.
Nell'analisi
per sottogruppi si sono valutate alcune ulteriori ipotesi. Ci si
aspettava una differenza significativa per bambini più grandi
(>12 mesi), con wheezing ricorrente, in base all'opinione
generalmente riconosciuta dell'efficacia degli steroidi nell'asma.
Tuttavia tale efficacia non è stata dimostrata, anzi c'è
un trend di maggiore efficacia nei bambini <12 mesi.
Si è
osservata una efficacia significativa sulla durata
dell'ospedalizzazione nei bambini RSV positivi. Tale evidenza è
in contrasto con quanto precedentemente ipotizzato dagli autori in
base a limitati dati ottenuti in vitro (Thomas 2002), ovvero che
bambini RSV positivi risponderebbero meno agli steroidi rispetto ai
bambini con malattia di altra eziologia virale.
Nel
gruppo trattato con dose giornaliera elevata (> 2 mg/kg/die di
prednisone equivalente) non si osserva un efficacia significativa, a
negare un effetto dose-dipendente per tali dosi. In contrasto, nel
sottogruppo trattato con dose totale di steroide >6mg/kg si
osserva un effetto significativo dello steroide, come per un
efficacia dose-dipendente. Tuttavia questi risultati vanno valutati
con cautela visto il piccolo numero di studi in ogni gruppo, l'
eterogeneicità di tipi e dosi e durata della terapia
steroidea. Nell'analisi inoltre non si prendono in considerazione
le differenze farmacologiche dei diversi tipi di steroide?, per
esempio la vita media del prednisone è significativamente più
breve di quella del desametasone.
L'eterogeneicità
degli studi merita un commento. In realtà nessuno studio è
comparabile per tipo di popolazione, interventi adottati e misure di
outcome. I due studi che valutano il desametasone ad alte dosi (1
mg/kg/die per 1-3 giorni) riportano risultati in evidente contrasto:
negativi in uno studio (Roosevelt 1996); estremamente positivi nel
secondo (Schuh 2002), con effetto drammatico sul tasso di
ospedalizzazione (7/36 dei tratti vs 15/34 non trattati) e
diminuzione dello Score Clinico a 4 ore. Tuttavia anche in questo
ultimo studio c'è contrasto tra il beneficio sul tasso di
ospedalizzazione e sullo score clinico, e l'assenza di beneficio
sulla frequenza respiratoria e la saturazione di ossigeno (misurata
sempre a 4 ore, come le score clinico).
Lo studio
di Van Woensel (Van Woensel 1997, bambini <1 mesi, tutti VRS
positivi) è unico per differenza di effetto tra i gruppi (a
favore dello steroide). E' da sottolineare comunque che i tassi di
ospedalizzazione in questo studio sono assai maggiori di quelli
riportati in studi anche dello stesso anno (Klassen 1997)
Esistono
inoltre incertezze relative agli outcome. La durata
dell'ospedalizzazione è l'outcome principale, ma i criteri
di ospedalizzazione non vengono definiti in alcun studio. Vengono
utilizzati 8 differenti score clinici, nessuno testato per validità,
accuratezza, riproducibilità, anche se l'RDAI (Respiratory
Distress Assessment Instrument) ha dimostrato una buona
riproducibilità. Inoltre gli Score sono stati misurati ad
intervalli di frequenza molto diversi (da ogni 30 minuti ad 1 volta
al giorno). Manca una misura che esprima la rilevanza clinica dello
score (valore predittivo verso durata dell'ospedalizzazione,
necessità di ossigeno. Migliore alimentazione etc )
Infine
alcune ricerche (Weinberger 2003) hanno fatto ipotizzare che gli
steroidi possano esprimere il massimo di efficacia nella fase
iniziale della malattia, prima della necrosi cellulare
Pochi
studi hanno osservato sistematicamente gli effetti collaterali degli
steroidi nei bambini con bronchiolite. Si deve quindi fare
riferimento ad altri studi, dai quali sembra che il rischio di
effetti collaterali sia comunque basso.
In
relazione all'uso diffuso di steroidi nei bambini con bronchiolite
ulteriori studi dovrebbero essere condotti. Per una adeguata
valutazione dell'effetto e per un'analisi di sottogruppi sono
attesi larghi campioni di studio. Un'attenzione alla durata di
malattia potrebbe chiarire ulteriori dubbi. L'analisi dei benefici
nei bambini con fattori di rischio per asma e atopia andrebbe inclusa
nell'analisi per sottogruppi. Andrebbero standardizzate le
definizione di outcome (in particolare i criteri per “ricovero” e
“ dimissione” e per l'utilizzo di interventi accessori e
sintomatici). Gli effetti collaterali andrebbero valutati
sistematicamente. Le misure di outcome dovrebbero essere scelte per
rilevanza clinica e validità.
In
assenza di evidenze sufficienti gli steroidi non sono al momento
indicati per i bambini affetti da bronchiolite.
Il
nostro commento
La
metanalisi della Cochrane è senz'altro la più
completa, per il numero di studi valutati ed in particolare per le
diverse variabili di popolazione e trattamento considerate. Ci sembra
di poter aggiungere poco al commento degli autori. Rispetto alla
metanalisi sull'adrenalina nella bronchiolite (Il
punto su, La Bronchiolite 1° parte) in questa revisione viene
fatta un'analisi per sottogruppi abbastanza soddisfacente, dalla
quale non emergono differenze statisticamente (e clinicamente)
significative. Rimangono aperti numerosi dubbi ed in particolare
quelli relativi all'effetto dose dipendente degli steroidi. Che gli
steroidi siano più efficaci in fase precoce di malattia è
un'ipotesi speculativa, ancora completamente da verificare. Un
ampio studio multicentrico per valutare l'efficacia dello steroide
era già stato auspicato da Garrison et al come conclusione
della prima revisione nel 2000. Si è calcolato che tale
studio, per avere una potenza necessaria, dovrebbe coinvolgere almeno
720 bambini. Ne vale davvero la pena?
