Un'ecografia
intestinale 'che parla'
1 Clinica
Pediatrica, IRCCS Burlo Garofolo, Trieste
2 U.O. di
Radiologia, IRCCS Burlo Garofolo, Trieste
E. è
una bambina di 4 mesi nata a termine dopo una gravidanza decorsa
regolarmente senza sofferenza perinatale. Allattata al seno con
crescita regolare fino alla sesta settimana di vita.
Successivamente presenta deflessione della curva ponderale con
l'avvio della supplementazione con latte di formula.
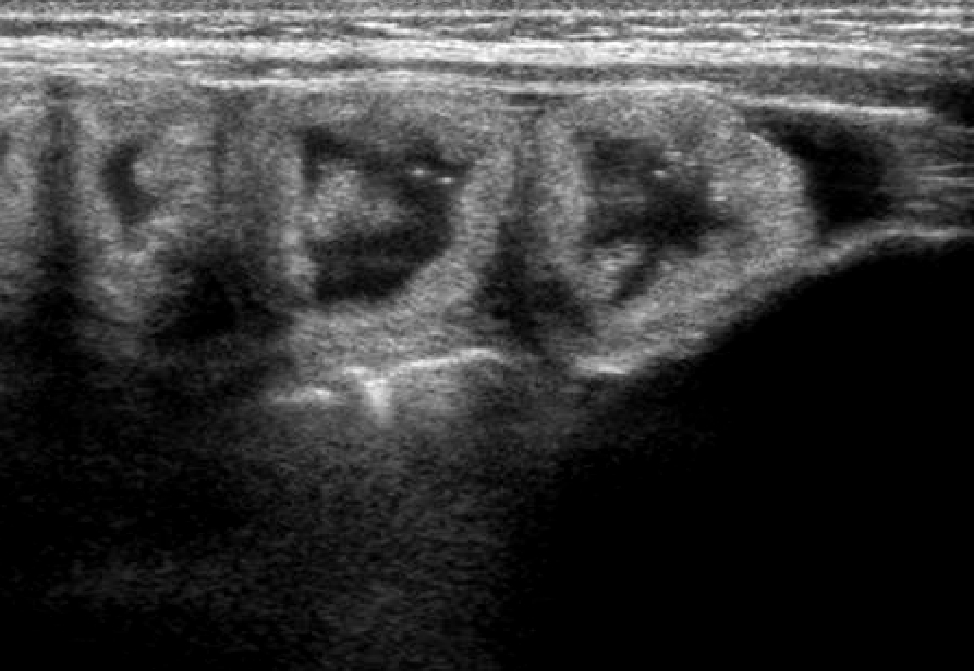
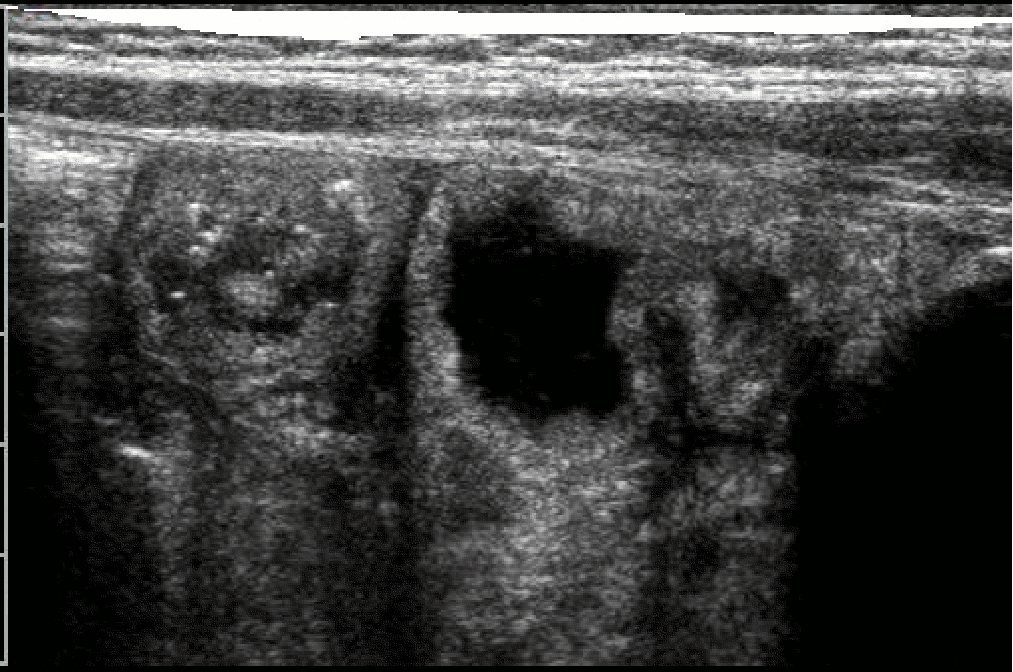
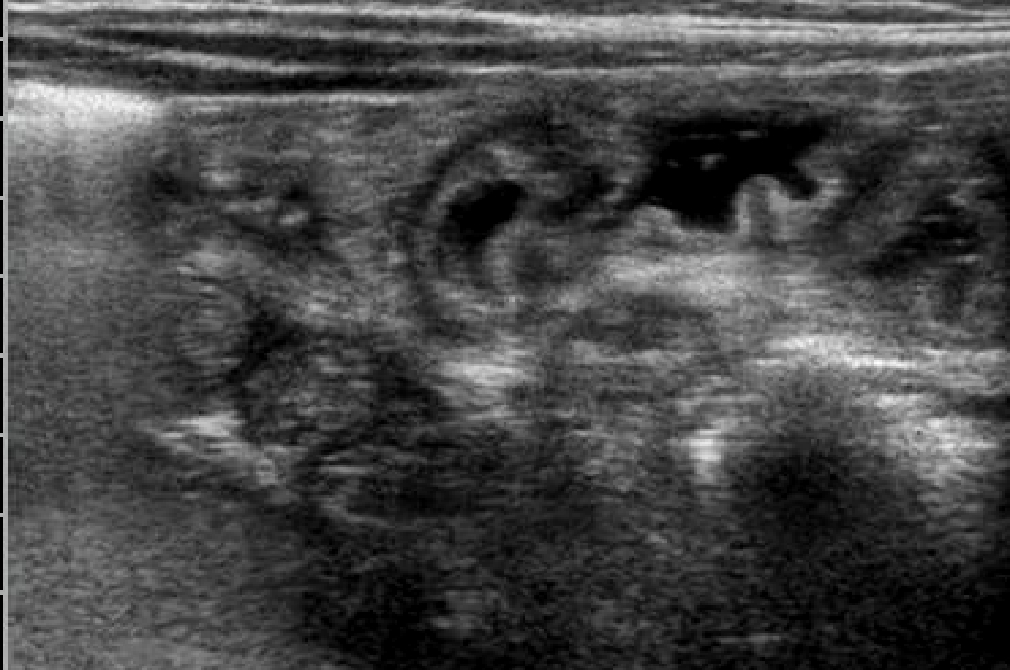
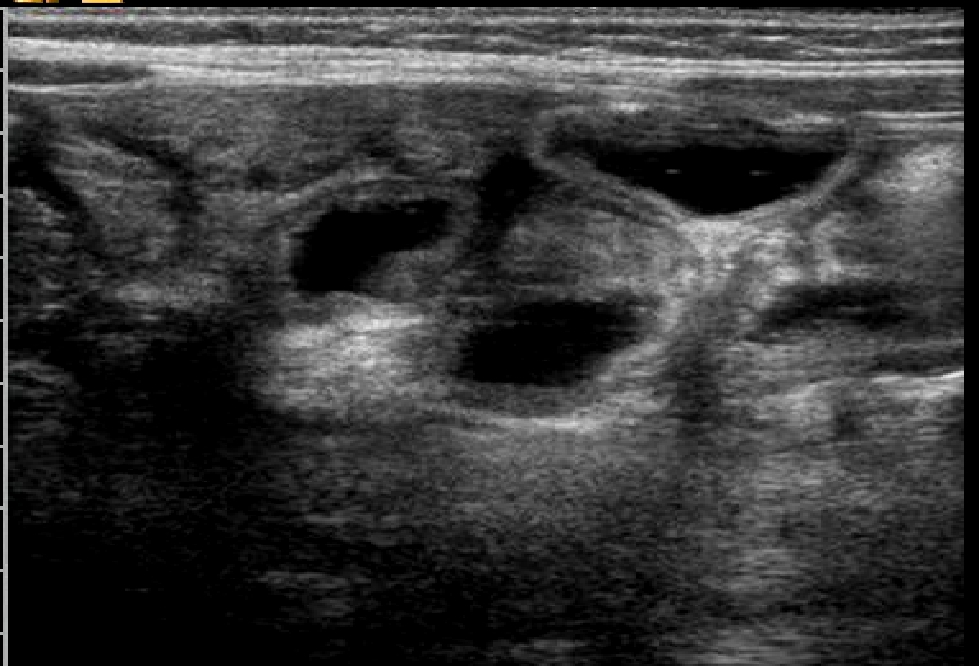
A 50 giorni di vita, dopo 4 giorni di alimentazione con formula lattea tipo 1, inizia a presentare episodi di vomito e scariche diarroiche che ne determinano il ricovero nel reparto di neonatologia del suo paese per un grave stato di disidratazione e distrofia. In occasione del ricovero si riscontra la presenza di addome molto globoso e teso, con successivo rilievo radiografico alla diretta dell'addome, di anse distese con parete diffusamente ispessita e di ascite. Gli esami di laboratorio evidenziano una severa ipoprotidemia (2.8mg/dl) e iposodiemia (Na 128mEq/L); viene eseguita paracentesi con riscontro liquido chiloso . Viene avviata nutrizione parenterale con rapido miglioramento delle condizioni generali, della crescita e del quadro ascitico ed intestinale . Il successivo decorso è però caratterizzato da una ripresa dei sintomi ad ogni tentativo di rialimentazione orale, anche con idrolisati spinti come il Neocate. Inefficace anche un tentativo terapeutico con octreotide. Nel sospetto di un'anomalia anatomica del sistema linfatico viene eseguita una linfo-scintigrafia che risulta negativa; nella norma anche l'esame ecocardiografico che esclude una pericardite costrittiva come pur remota possibile causa, e lo studio del tubo digerente con pasto baritato che nega una malrotazione ( altra possibile eziologia dell'ascite chilosa). Da segnalare il riscontro di un'ipereosinofilia periferica (1800/mm3) e di eosinofili fecali. E. giunge quindi alla nostra attenzione per completare l'iter diagnostico, già avviato dai colleghi, nel sospetto di un'anomalia del sistema linfatico intestinale. All'ingresso si presenta in discrete condizioni generali, distrofica, con cute pallida e marezzata; l'addome è moderatamente disteso, ma trattabile; non presenti edemi declivi. Un'ecografia addominale conferma un diffuso ispessimento della parete intestinale e la presenza di una piccola falda ascitica. (fig.1-2) Gli
esami di laboratorio eseguiti evidenziano un quadro di
ipoprotidemia (proteine totali 3.9), ipogammaglobulinemia (IgG
103, IgA 14, IgM 32) e leucopenia (GB 3930) con marcata riduzione
dei linfociti CD4 (CD4 16%) ed inversione del rapporto CD4/CD8,
compatibile con il sospetto diagnostico principale di
linfangiectasia intestinale (probabilmente l'inversione del
rapporto è legata ad un trasporto selettivo dei CD4 nei
fluidi linfatici); confermata, seppur in calo, la presenza di
ipereosinofilia periferica (eosinofili 750); un carico di
trigliceridi risulta piatto; negativi, infine i test di
valutazione dell'assorbimento intestinale: xilosemia,
alfa1antitripsina fecale.
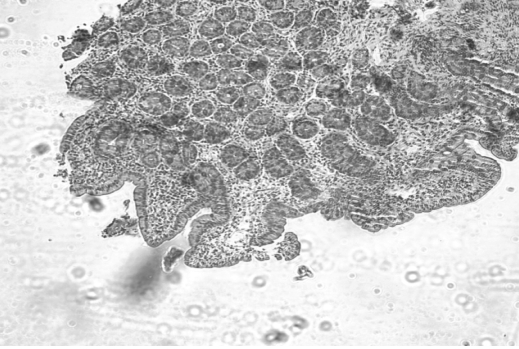
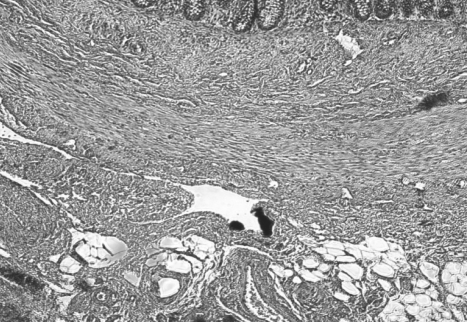
Nonostante il forte orientamento diagnostico prendiamo in considerazione ed escludiamo tutte le possibili cause di enteropatia protido-disperdente e di malassorbimento comprese la fibrosi cistica (test del sudore negativo) e le cause infettive (ricerca dei parassiti fecali, PCR per CMV, mantoux tutte negative). Una radiografia e un clisma opaco ci consentono nuovamente di escludere malrotazioni e altre malformazioni intestinali che rientrano tra le possibili cause di linfangectasia. La biopsia duodenale mostra una mucosa di tipo 3B con villi corti a base ampia e rarefatti come da patologia malassorbitiva; presenti i microvilli; evidenza di fitto infiltrato linfoplasmacellulare e localmente eosinofilo del corion con ectasie linfatiche polifocali (fig. 3) La
laparoscopia esplorativa eseguita dopo assunzione orale di un
pasto grasso (latte di soja) tinto con un colorante alimentare ha
evidenziato diffusa trasudazione del chilo attraverso la parete
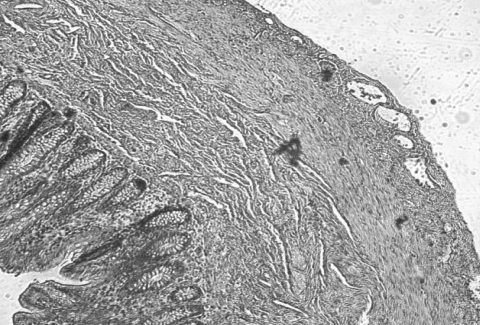
intestinale. Sono risultate infine dirimenti le sezioni
istologiche che hanno messo in luce l'ectasia dei vasi
linfatici. (fig.
4)
La
diagnosi quindi di linfangectasia intestinale diffusa poteva
essere confermata.
La terapia elettiva per questa patologia è la nutrizione parenterale a lungo termine (alcuni mesi almeno) che avviamo dopo posizionamento di catetere venoso centrale; l'alimentazione orale prevede esclusivamente l'assunzione di cibi privi di grassi e proteine; utile l'impiego degli MCT per la ragione prima esposta. Dopo
l'avvio della NP e dell'alimentazione orale con cibi privi di
grassi e proteine assistiamo ad una rapida normalizzazione del
quadro ecografico intestinale con normalizzazione dello spessore
di parete e risoluzione del versamento ascitico (fig.5-6)
e ad un miglioramento dei valori ematici: aumento dei linfociti
(1300), normalizzazione delle sottopopolazioni linfocitarie ( CD3
43%, CD4 38%, CD8 14%, CD 1925%, NK 21%) e del profilo
immunoglobulinico (IgG 593, IgA 14, IgM 49); rialzo anche della
protidemia a 5.9.
Di regola questa è una patologia malformativa primitiva, che trova nel tempo un suo compenso ed equilibrio con la nutrizione parenterale e con la crescita. Peraltro in questo caso la comparsa della prima manifestazione della malattia 4 giorni dopo l'assunzione di latte di formula, il rilievo bioptico di enteropatia con infiltrato eosinofilo ci hanno fatto sospettare un possibile ruolo dell' allergia alle proteine del latte vaccino nella genesi del quadro. CONTRIBUTO
La
linfangectasia intestinale è una rara condizione dovuta
alla dilatazione e rottura dei vasi linfatici del tratto
gastrointestinale, più frequentemente a carico del piccolo
intestino, con una distribuzione segmentale, multifocale o
diffusa. Viene diagnosticata di solito in bambini o giovani come
conseguenza di una anomalia congenita del sistema linfatico.
Occasionalmente, la linfangectasia intestinale può esser
vista anche nella popolazione adulta, ma generalmente secondaria
a cause di compressione linfatica. In base alla sua eziologia, la
linfangectasia intestinale può esser così
classificata in una forma primitiva ed una secondaria [1-3].
Quella primitiva, congenita, di solito si associa ad altre
sindromi genetiche, come la Sindrome di Turner [2,8];
al contrario quella secondaria è acquisita, dovuta a
disordini gastrointestinali e patologie intra-addominali e
retroperitoneali: come carcinoma, linfoma, tubercolosi o
pericarditi costrittive, fibrosi retroperitoneali, ripetute
infezioni parassitarie [1,4-6].
La linfangectasia intestinale clinicamente si presenta in modo similare in entrambe le forme, con una grande varietà di segni e sintomi a seconda del grado di estensione del danno. Alcuni pazienti possono essere del tutto asintomatici, mentre nella maggior parte dei casi la malattia si presenta come una grave enteropatia proteino disperdente, oppure come un ritardo di crescita oppure sotto forma di ricorrenti emorragie del tratto gastrointestinale [1,2,9]. I pazienti possono anche presentare un'epigastralgia diffusa, diarrea cronica, steatorrea, edema, ascite chilosica e linfocitopenia. La linfocitopenia si caratterizza per la presenza di livelli di linfociti CD4 marcatamente diminuiti con CD8 normali od aumentati, con conseguante inversione del rapporto CD4/CD8, questo potrebbe esser dovuto alla presenza di un trasporto di tipo selettivo dei CD4 nei linfatici oppure per un tempo di emivita più breve dei CD8 rispetto ai CD4 [1,2]. La diagnosi di certezza si basa sulle caratteristiche istologiche che consistono nella presenza di linfatici intra e submucosali dilatati. Pertanto è dirimente l'esecuzione di una laparoscopia con prelievo bioptico [7]. Il trattamento dipende dalla severità e dal grado di estensione della patologia. Per la maggior parte dei pazienti con la forma congenita il gold-standard consiste nell'esecuzione di una paracentesi per il drenaggio dell'ascite chilosa e contemporaneo avvio di una nutrizione parenterale associata a dieta priva di grassi, con un'elevata quota di proteine e supplementazione di trigliceridi a media catena [1,2]. Molto spesso questo approccio di “messa a riposo” permette una favorevole evoluzione del quadro clinico con verosimile interruzione di un circolo vizioso dilatazione-perdite e sviluppo di un compenso o di una maturazione favorevole della lesione, sufficiente a permettere una autonomia intestinale. In casi, non responsivi a tale trattamento conservativo, emerge dalla letteratura la possibilità di associare alla NP la somatostatina. Quest'ultima induce un minor assorbimento di grassi, minor concentrazione di trigliceridi nel dotto toracico ed attenua il flusso linfatico nei linfatici maggiori. In aggiunta, riduce le secrezioni gastriche, pancreatiche ed intestinali, inibisce la motilità dell'intestino, rallenta il processo di assorbimento intestinale e il flusso sanguigno splancnico. In conclusione, l'azione della somatostatina sembrerebbe quella di ridurre l'escrezione del liquido linfatico agendo direttamente su specifici recettori normalmente presenti sulla parete dei vasi linfatici intestinali [13,14]. Di fatto nel nostro caso la somatostatina era già stata usata senza beneficio. L'approccio invasivo è riservato esclusivamente ai quadri di pertinenza chirurgica, quali ad esempio malrotazione intestinale, cause compressive e persistenza di fistola non responsiva al trattamento di associazione tra NP e somatostatina [2,10-12] oppure lesioni segmentarie. Bibliografia
1. Browse NL, Wilson NM et al. Aetiology and treatment of chylous ascites. Br J Surg 1992; 79:1145-50 2. Liebovitch I. Postoperative chylous ascites the urologist's view. Drugs Today 2002; 38:687-697 3. Press OW et al. Evaluation and management of chylous ascites. Ann Intern Med 1982; 96:358-364 4. Halkic N et al. Postoperative chylous ascites after radical gastrectomy. A case report. Minerva Chir 2000, 58:389-391 5. Warner RR, Croen EC, et al. A carcinoid tumor associated with chylous ascites and elevated tumor markers. Int J Colorectal Dis 2002; 17:156-160 6. Amin R. Chylous ascites from prostatic adenocarcinoma. Urology 2002; 59:773 7. Senyuz OF et al. Chylous ascites after liver transplantation with mesentero portal jump graft. J Hepatobiliary Pancreat Surg 2001; 8:571-572 8. Shafizadeh SF, et al. Chylous ascites secondary to laparoscopic donor nephrectomy. Urology 2002; 60:345 9. Bacelar TS et al. Postoperative chylous ascites: a rare complication of laparoscopic Nissen fundoplication. JSLS 2003; 7:269-271 10. Aalami OO, et al. Chylous ascites: a collective review. Surgery 2000; 128:761-778 11. Leibovitch I et al. The diagnosis and management of postoperative chylous ascites. J Urol 2002; 167:449-457 12. Lee YY et al. Total parenteral nutrition as a primary therapeutic modality for congenital chylous ascites: report of one casa. Acta Pediatr Taiwan 2002; 43:214-216 13. Shapiro AM et al. Rapid resolution of chylous ascites after liver transplantation using somatostatin analog and total parenteral nutrition. Transplantation 1996; 61:1410-1411 14. Reubi JC et al. Preferential location of somatostatin receptors in germinal centers of human gut lymphoid tissue. Gastroenterology 1992; 103:1207-1214 |
Evidenza
di diffuso ispessimento a tutto spessore delle pareti intestinali
.
Parete
duodenale con mucosa di tipo 3B con villi corti e rarefattite
Tessuto
appendicolare con presenza di piccole ectasie di strutture
linfatiche intramurali.
Normalizzazione
del quadro con riduzione dello spessore di parete e risoluzione
del versamento ascitico
|